Quando la Normal Science fallisce: una anomalia clinica che apre il problema
Quando la Normal Science fallisce: una anomalia clinica che apre il problema
|
Autore principale |
|
|
Co-autori |
|
|
Aree di contributo |
sviluppo concettuale del limite della Normal Science - Interpretazione clinica di anomalie diagnostiche non eliminabili - Fondazione epistemologica del modello diagnostico quantum-like |
|
Questo capitolo fa parte di un lavoro in evoluzione. Aree di contributo e collaboratori possono ampliarsi in revisioni future. | |
Abstract:
Questo capitolo chiude la fase di Normal Science esaminando una vulnerabilità diagnostica centrale nel Dolore Orofacciale (OP) e nei Disordini Temporo-Mandibolari (TMD): il rischio di scambiare un quadro clinico “TMD-like” con condizioni sistemiche e neurologiche in grado di mimarlo, soprattutto nelle fasi iniziali. A partire da un follow-up clinico prospettico di 5 anni, introduciamo il fondamento concettuale dell’Indice Ψ come paradigma diagnostico orientato alla gestione dell’incertezza, nel quale l’esito dipende non solo da “quale test” viene eseguito, ma anche da quando e in quale ordine l’informazione viene acquisita.
In una prima fase, l’aggiornamento bayesiano viene applicato a un percorso diagnostico basato su RDC/TMD, ottenendo un’elevata probabilità condizionale di TMD quando l’output RDC risulta positivo all’interno della coorte sintomatica. Tuttavia, il follow-up a lungo termine rivela che molti pazienti sintomatici inizialmente classificati come TMD erano in realtà portatori di gravi condizioni non-TMD. Ne deriva una distorsione “di tipo interferenziale” della certezza diagnostica: un calo quantitativo dall’81% al 9,56% in un modello contestuale, usato qui per formalizzare la transizione epistemologica dalla commutabilità deterministica alla non-commutatività clinica (effetti d’ordine).
Il capitolo conclude sostenendo che il formalismo diagnostico deterministico è insufficiente nelle condizioni multifattoriali e che la ricerca clinica futura dovrebbe esplorare cornici probabilistiche contestuali e quantum-like come strumenti per modellare effetti d’ordine, interferenza diagnostica e incertezza ad alto impatto clinico.
Introduzione
Raggiungiamo la fine della sezione Normal Science (in termini kuhniani: una fase matura di “puzzle-solving” sotto un paradigma dominante), nella quale lo status quo attuale in OP e TMDs è stato presentato insieme a un insieme di vulnerabilità diagnostiche non risolte. Queste vulnerabilità non sono ancora “anomalie” nel senso kuhniano stretto, ma sono punti critici che minacciano in modo sistematico la sicurezza diagnostica e la tempestività.
Le condizioni croniche di OP sono difficili da diagnosticare e trattare perché i meccanismi di eziologia e patogenesi rimangono solo parzialmente compresi.[1][2] Una caratteristica frequente dell’OP è la sua natura multifattoriale: il dolore correlato ai TMDs spesso si sovrappone a sintomi e segni che possono anche essere manifestazioni precoci di malattie neurologiche o sistemiche, rendendo complessa la diagnosi differenziale.[3][4][5][6]
Nei pazienti con disturbi funzionali del sistema stomatognatico sono stati riportati fattori di rischio periferici (incluse variabili occlusali)[7][8][9][10][11][12] così come fattori di rischio centrali biopsicosociali che coinvolgono disfunzioni del SNC.[13][14] Tuttavia, questi quadri non hanno risolto i meccanismi causali né generato un miglioramento decisivo nella gestione clinica; di conseguenza persiste un’ampia gamma di trattamenti prevalentemente conservativi.[15][16][17][18][19]
Un ostacolo rilevante nella diagnosi differenziale OP/TMD rimane l’instabilità di criteri standardizzati per definire sottotipi di TMD, storicamente affrontata attraverso lo sviluppo dei Research Diagnostic Criteria (RDC). Per un inquadramento su RDC, vedi il capitolo dedicato.
Lo studio prospettico qui presentato costituisce il ponte verso il paradigma dell’Indice Ψ. La coorte è stata valutata longitudinalmente in tre fasi clinicamente distinte:
- — fase diagnostica preliminare
- — fase diagnostica avanzata (dopo follow-up e rivalutazione esperta)
- — chiusura diagnostica definitiva (modellazione del protocollo: Indice , letto “Indice ket Psi”)
Poiché il primo step è incardinato sull’aggiornamento bayesiano, richiamiamo il formalismo minimo.
Teorema di Bayes (richiamo minimo)
Il teorema di Bayes aggiorna la probabilità di un’ipotesi alla luce di un’evidenza:
dove:
- — ipotesi (ad es. “TMD presente”)
- — evidenza (ad es. “output RDC positivo”)
e:
Nota clinica importante: nella pratica diagnostica, le probabilità vengono spesso calcolate su una coorte selezionata (ad es. pazienti sintomatici che entrano in un percorso), non sulla popolazione generale. Per questo la prevalenza deve essere definita rispetto alla coorte in analisi.
Indice al tempo (certezza bayesiana nella coorte sintomatica)
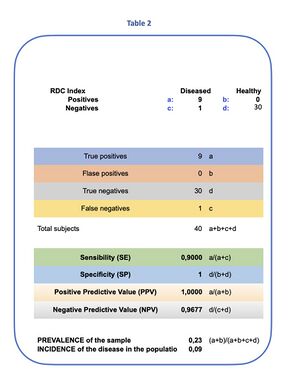
Al tempo , il modello RDC viene applicato a un campione di 40 soggetti (30 asintomatici, 10 sintomatici). All’interno della coorte sintomatica, 9 soggetti sono classificati come TMD-positivi secondo RDC, mentre 1 soggetto sintomatico è classificato come non-TMD secondo RDC (Tabella 1).
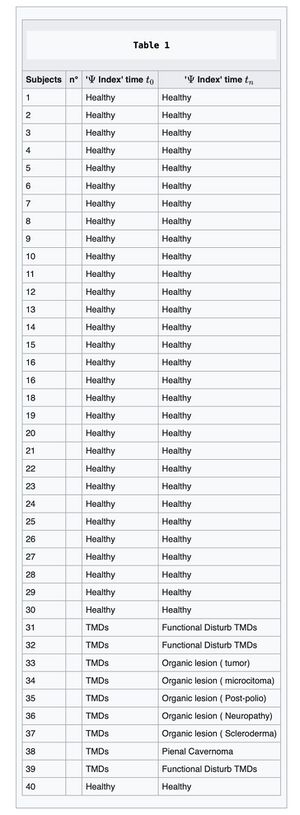
Per evitare una fuorviante “prevalenza di popolazione”, definiamo esplicitamente:
- Coorte = pazienti sintomatici che entrano nel percorso diagnostico (n=10)
- = “TMD (come classificato dal modello RDC al tempo )”
- = “output del test RDC positivo”
Dalla coorte:
- Sensibilità (osservazionale/assunta per il percorso RDC in questa coorte):
- Specificità (osservata/assunta in questo dataset): , dunque
Allora:
e:
Quindi, nella coorte sintomatica e sotto queste condizioni, un output RDC positivo produce una classificazione TMD apparentemente “certa”.
È qui che emerge il rischio epistemologico: una certezza probabilistica può essere prodotta all’interno di un modello anche quando il ground truth clinico (eziologia e rischio sistemico) non è allineato allo spazio ipotetico del modello.
Per esempio, scenari clinicamente complessi possono mimare pattern OP/TMD e confondere la classificazione.[20]
Per questo motivo, i soggetti sintomatici sono stati rivalutati da un team multidisciplinare e seguiti longitudinalmente. La fase avanzata al tempo modifica il paesaggio diagnostico.
Indice al tempo (effetti d’ordine e non-commutatività diagnostica)
Il follow-up e la rivalutazione esperta rivelano che molti soggetti sintomatici erano portatori di gravi patologie non-TMD (ad es. meningiomi, cavernomi pineali, sclerodermia, emispasmo emimasticatorio). Queste condizioni erano già discusse nei capitoli di Normal Science, ma la loro comparsa all’interno di una coorte “RDC-TMD positiva” costituisce una reale pressione epistemologica sul paradigma.
Il pensiero diagnostico classico assume spesso commutabilità: variabili e test possono essere permutati senza cambiare significato. Clinicamente, però, il tempo crea un ordine: l’evoluzione della lesione, l’emergere dei sintomi e la sensibilità dei test sono dipendenti dal tempo. Di conseguenza, l’ordine con cui l’informazione viene acquisita può modificare l’esito diagnostico.
Esempio paradigmatico (prudente): dipendenza temporale e sequenziale
Un esempio clinico minimale rende intuitivo il punto senza forzare conclusioni: a parità di sintomatologia riferita (bruxismo/dolore oro-facciale), la lettura clinica può cambiare in modo sostanziale quando cambiano il tempo e l’ordine con cui vengono acquisiti i blocchi informativi.
- Nel 2000: un percorso odontoiatrico standard (criteri tipo-RDC e test orientati al contesto TMD) produce una classificazione coerente localmente: “TMD/bruxismo”.
- Nel 2014: un approfondimento neurofisiologico, eseguito in una fase più avanzata e con maggiore potere discriminante per alcuni quadri trigeminali, produce dati compatibili con uno scenario eziologico diverso e impone una rivalutazione differenziale.
In questa sede l’esempio non viene usato per sostenere che un singolo test “diagnostichi” una specifica patologia, ma per introdurre un fatto clinicamente cruciale: l’esito diagnostico può dipendere non solo da quali informazioni sono disponibili, ma anche da quando e in quale sequenza vengono acquisite.
In termini operativi, possiamo descrivere il percorso come applicazione sequenziale di due blocchi:
- = blocco odontoiatrico standard (lettura locale TMD/RDC)
- = blocco neurofisiologico/sistemico (lettura di livello superiore, differenziale)
e ammettere esplicitamente che tra e intercorra un tempo :
Quando il sistema è complesso e a fasi sovrapposte, non è affatto garantito che l’inversione dell’ordine sia neutra:
La formalizzazione completa di questo punto (non-commutatività diagnostica come dipendenza dell’esito da ordine e tempo) viene sviluppata nel capitolo dedicato: Variabili non commutative in clinica.
Perché serve un indice di stato
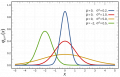
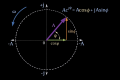
I risultati presentati indicano che l’esito diagnostico non può essere adeguatamente rappresentato come un singolo valore numerico scalare. Ciò che conta, nei sistemi clinici complessi, non è soltanto l’intensità di un indice, ma la configurazione complessiva dello stato del sistema: modulo, fase, orientamento informazionale e dipendenza dal percorso osservativo.
Un modello puramente scalare consente di ordinare i dati lungo una sola dimensione (ad esempio “più” o “meno” patologico), ma non è in grado di distinguere stati clinicamente differenti che condividono lo stesso valore numerico. In questi casi, la coincidenza del valore non implica equivalenza di stato.
È in questo contesto che emerge l’esigenza di un indice di stato mesoscopico, di natura vettoriale, capace di rappresentare il sistema clinico come configurazione e non come semplice classificazione binaria sano/malato. Un tale indice non descrive soltanto “quanto” un fenomeno è presente, ma “come” esso è organizzato all’interno del sistema clinico osservato. (Figura 1,2)
Detto questo, prima di introdurre una rappresentazione vettoriale dello stato clinico, è opportuno esaminare i limiti operativi che si manifestano all’interno di un modello statistico classico consolidato nella pratica scientifica: il Teorema di Bayes.
Formalizzazione contestuale quantum-like (toy model) — guida di lettura
Nota metodologica: le matrici seguenti sono un toy model introdotto per rendere esplicito l’effetto d’ordine. Non sono stime empiriche dirette: i coefficienti sono parametri didattici scelti per rendere visibile la dipendenza dalla sequenza informativa.
1) Stati e vettore di stato
Per semplicità consideriamo due stati clinici:
- = “sano / assenza di evidenza di ipereccitabilità trigeminale”
- = “patologico / evidenza di ipereccitabilità trigeminale”
Rappresentiamo lo “stato” del paziente come un vettore:
dove e sono pesi (qui trattati come probabilità/credence) e soddisfano .
Al baseline assumiamo:
(cioè: all’inizio il sistema è considerato “sano”).
2) Come si legge una matrice-test
Ogni test è rappresentato da una matrice che aggiorna il vettore di stato:
Convenzione di lettura:
- le colonne rappresentano lo stato “in ingresso” (prima del test),
- le righe rappresentano lo stato “in uscita” (dopo il test).
Quindi il coefficiente indica quanto il test sposta il peso da verso .
3) Operatore EMG (bassa discriminazione precoce)
Assumiamo un EMG poco discriminante nelle fasi precoci:
Applicazione al baseline:
Lettura: dopo EMG il sistema resta “prevalentemente sano” (), con una piccola quota su ().
4) Operatore rcIMR (alta discriminazione)
Assumiamo un test rcIMR ( ciclo di recupero del Riflesso Inibitorio Masseterino) altamente discriminante:
Applicazione allo stato dopo EMG:
Lettura: dopo rcIMR il peso si sposta su ().
Questo rende visibile l’effetto d’ordine: la sequenza EMG→rcIMR produce un esito diverso rispetto al caso in cui rcIMR sia eseguito come primo test.
5) Scenario 2: rcIMR come primo test
Se rcIMR viene eseguito subito:
Interpretazione clinica: l’uso precoce di un test più discriminante può far emergere lo stato patologico prima, riducendo il ritardo diagnostico.
Probabilità classica vs probabilità quantum-like (interferenza contestuale)
La probabilità classica (Kolmogorov, 1933)[21] descrive gli eventi come insiemi e assegna a ciascun evento un “peso” numerico tra 0 e 1.
1) Additività: cosa significa “eventi disgiunti”
Due eventi sono disgiunti quando non possono accadere insieme (non si sovrappongono). Esempio semplice: in una singola estrazione, “esce 3” e “esce 5” sono disgiunti.
In questo caso vale la regola additiva:
- significa “accade oppure accade ”.
- Quindi: se e non possono coesistere, la probabilità dell’“uno o l’altro” è la somma delle due.
2) La formula della probabilità totale: scomporre un problema complesso in casi semplici
Spesso vogliamo calcolare la probabilità di un evento (per esempio: “test positivo”). Ma può verificarsi per motivi diversi: dipende dal fatto che il paziente appartenga a classi differenti .
La formula classica della probabilità totale dice:
Lettura passo per passo:
- è una variabile che separa i casi possibili (es. classi cliniche).
- indica uno specifico caso (una specifica classe).
- è “quanto spesso” capita quel caso (la sua frequenza/probabilità).
- è la probabilità che osserviamo se siamo nel caso .
- La somma significa: “metto insieme tutti i casi possibili”.
In altre parole: → calcolo come media pesata dei vari scenari .
Esempio clinico classico: come l’incidenza modifica il risultato bayesiano
Consideriamo un esempio volutamente semplice, tratto dalla pratica clinica quotidiana dei TMDs.
Supponiamo:
- una popolazione generale in cui la prevalenza dei TMDs è circa del 30%
(dato compatibile con molte stime epidemiologiche).
- un test diagnostico (es. criteri tipo-RDC) con:
* sensibilità
* specificità
Dove:
- = “il soggetto ha un TMD”
- = “il test risulta positivo”
Caso 1: popolazione generale (prevalenza 30%)
Poniamo:
Calcoliamo la probabilità di un test positivo:
Ora la probabilità che un soggetto con test positivo abbia realmente un TMD è:
Caso 2: popolazione a bassa prevalenza (prevalenza 9%)
Supponiamo ora di applicare lo stesso test in una popolazione in cui i TMDs sono relativamente rari (ad esempio una popolazione generale non selezionata), con una prevalenza del 9%.
Poniamo:
Calcoliamo la probabilità di un test positivo:
Ora calcoliamo la probabilità che un soggetto con test positivo abbia realmente un TMD:
Lettura clinica immediata
Il test è identico al caso precedente. Sensibilità e specificità non cambiano.
Eppure:
- con prevalenza del 30% →
- con prevalenza del 9% →
Un test “buono” può quindi produrre **un risultato clinicamente debole** quando applicato in un contesto a bassa incidenza.
Lettura clinica semplificata
Il test è **lo stesso**. Sensibilità e specificità **non cambiano**.
Eppure:
- nella popolazione generale ( esempio riportato in tabella su 40 soggetti) un test positivo significa “79% di probabilità di TMD”;
- nella popolazione selezionata ( stesso esempio ma su 10 soggetti sintomatici) significa “93% di probabilità di TMD”.
Questo mostra un punto chiave: la probabilità diagnostica non è una proprietà del test, ma del **contesto in cui il test viene applicato**. Ciò significa che: a parità di test, un risultato positivo non ha un significato diagnostico assoluto, ma dipende dalla popolazione in cui il test viene applicato.
In una popolazione a bassa prevalenza di TMD, un test positivo fornisce una certezza limitata;
in una popolazione già selezionata, lo stesso risultato produce una certezza molto maggiore.
Già nel modello bayesiano classico, quindi, il risultato numerico dipende dalla popolazione, dalla selezione e dalla storia osservativa.
Oltre Bayes: quando la probabilità classica non basta
A questo punto emerge un limite strutturale del ragionamento bayesiano classico, che è importante rendere esplicito.
Supponiamo di trovarci di fronte a un paziente che presenta una sintomatologia dolorosa pienamente compatibile con un TMD e che, all’interno del percorso odontoiatrico standard, produce un output positivo ai test diagnostici disponibili. In un quadro bayesiano classico, questa informazione tende ad aumentare progressivamente la probabilità a posteriori dell’ipotesi “TMD”, soprattutto quando il paziente appartiene a una popolazione già selezionata.
Tuttavia, esiste una possibilità clinicamente cruciale: che quel paziente presenti sì una sintomatologia odonto-facciale compatibile con un TMD, ma che l’eziologia reale del dolore sia diversa e più grave, ad esempio una patologia neurologica come un cavernoma pineale.
Nel formalismo bayesiano standard, questa eventualità può essere gestita solo ampliando lo spazio delle ipotesi e ricalcolando le probabilità su classi alternative. Ma così facendo si assume implicitamente che le diverse ipotesi eziologiche contribuiscano in modo indipendente e additivo alla probabilità finale.
Il problema è che, in questi scenari clinici, le ipotesi non sono semplicemente alternative: esse **interagiscono**, competono per spiegare gli stessi segni clinici e possono produrre sovrapposizioni sintomatologiche tali da generare una falsa sensazione di certezza diagnostica.
In altre parole, la presenza di una patologia non-TMD grave non si limita ad aggiungere una nuova ipotesi, ma può **ridurre** l’affidabilità dell’interpretazione TMD, pur in presenza di test positivi. Questo effetto non è rappresentabile come una semplice sottrazione o redistribuzione di probabilità nel modello classico.
È qui che si introduce l’idea di un termine correttivo: un contributo che non si somma in modo lineare, ma che può **attenuare** (o, in altri contesti, amplificare) la probabilità classica risultante.
Questo termine, che nel linguaggio formale viene detto “interferenza”, non implica alcuna trasposizione fisica della meccanica quantistica in medicina. Esso rappresenta invece un modo matematicamente controllato per descrivere l’effetto del contesto, della competizione eziologica e dell’ordine informativo sul risultato diagnostico.
Su queste basi diventa possibile introdurre un formalismo probabilistico di tipo quantum-like, concepito non per sostituire Bayes, ma per estenderlo nei casi in cui la probabilità classica, pur correttamente applicata, non riesce a rappresentare la reale instabilità dello stato clinico.
Questo fenomeno non è un artificio matematico, ma una descrizione compatta di un’esperienza clinica reale.
3) Perché introdurre un termine “quantum-like”
Nei sistemi complessi (come in clinica), l’esito può dipendere dal contesto e dall’ordine con cui le informazioni vengono acquisite. Quando questo accade, la semplice “somma di casi” può non descrivere bene ciò che vediamo nella pratica.
Per rappresentare questa dipendenza contestuale, un formalismo quantum-like introduce un termine correttivo, detto “di tipo interferenziale”. Attenzione: qui “interferenza” non significa che c’è fisica quantistica nel paziente, ma che i contributi informativi dei diversi casi possono combinarsi in modo non puramente additivo.
4) La formula quantum-like: stessa base + un correttivo
La formula si scrive come:
Spiegazione naif della Parte aggiuntiva
- significa: “non sommo un caso alla volta, ma considero le coppie di casi”.
(cioè: come interagiscono due classi possibili quando il contesto è ambiguo).
- La radice quadrata serve a costruire un termine “simmetrico” tra i due contributi.
È un modo standard per combinare due pesi probabilistici senza privilegiare uno dei due.
- è un parametro che modula la correzione:
'se è positivo' la correzione aumenta il valore finale;
'se è negativo' la correzione lo riduce;
'se è zero' la correzione si annulla e si torna al modello classico.
- Il fattore è parte della forma canonica del termine interferenziale: non cambia il significato concettuale, serve solo a mantenere la simmetria della costruzione.
In sintesi:
- La Parte 1 è la probabilità totale “standard”.
- La Parte 2 aggiunge (o sottrae) un contributo che rappresenta l’effetto del contesto: sovrapposizione, ambiguità, ordine informativo, competizione tra classi.
Questo è il motivo per cui il modello è detto “quantum-like”: non perché applica la fisica quantistica ai tessuti, ma perché usa una struttura matematica capace di rappresentare effetti non additivi tipici dei sistemi complessi.
Dati dal follow-up al tempo (reinterpretazione contestuale)
Dal punto di vista del follow-up, la coorte sintomatica (n=10) contiene:
- soggetti inizialmente classificati come TMD da RDC al tempo : 9
- soggetti successivamente riconosciuti come portatori di gravi patologie non-TMD nella stessa coorte sintomatica: 7
Questo indica che “RDC positivo” non mappa necessariamente su una “classe eziologica reale” nei pazienti OP medicalmente complessi. In altre parole: lo spazio-obiettivo del paradigma è incompleto e tale incompletezza genera una distorsione sistematica.
Definiamo (per il calcolo contestuale):
- probabilità che un soggetto della coorte sintomatica appartenga alla classe “RDC-TMD” al tempo .
- probabilità di ottenere un output RDC positivo dato che il soggetto appartiene alla classe RDC-TMD (sensibilità del percorso RDC nella coorte considerata).
- probabilità che, all’esito del follow-up e della rivalutazione esperta, un soggetto della stessa coorte sintomatica appartenga a una classe non-TMD grave (patologie neurologiche o sistemiche con mimica TMD).
- parametro illustrativo che codifica la discrepanza diagnostica tra le due letture eziologiche concorrenti ( e ).
In questo contesto non rappresenta un angolo fisico misurato sul paziente, ma un indicatore formale del grado di conflitto tra due spiegazioni cliniche che producono un quadro sintomatologico simile.
- Il valore corrisponde alla scelta didattica di , utilizzata per rappresentare un caso di interferenza negativa “forte ma non massima”, in cui la presenza di una eziologia non-TMD grave riduce in modo sostanziale la certezza diagnostica ottenuta nel modello classico.
Termine vero-positivo (classico)
Termine correttivo “interferenziale” (contestuale)
Efficacia contestuale
Interpretazione: il percorso RDC può produrre un’elevata certezza interna per la “classificazione TMD” pur non proteggendo il paziente rispetto a eziologie non-TMD gravi. Il collasso da 81% a 9,56% formalizza il gap di paradigma: quando lo spazio diagnostico è incompleto, la certezza diventa fragile e dipendente dall’ordine dell’informazione.
Un risultato controintuitivo (ma clinicamente cruciale)
Il risultato ottenuto può apparire paradossale e persino inquietante: da una probabilità bayesiana interna pari all’81% per la classificazione TMD (all’interno della coorte sintomatica), il modello contestuale produce una probabilità effettiva di circa 9.56%.
È fondamentale chiarire che questo “crollo” non indica un errore matematico, né un fallimento del test RDC in sé. Al contrario, esso mette in luce una fragilità epistemologica: una probabilità elevata può essere perfettamente coerente **dentro un modello incompleto** e tuttavia risultare clinicamente fuorviante.
Nel modello bayesiano classico, la certezza cresce perché l’ipotesi “TMD” viene aggiornata all’interno di uno spazio eziologico che non contempla in modo adeguato patologie alternative capaci di mimarne il quadro sintomatologico. La probabilità a posteriori risponde correttamente alla domanda posta dal modello, ma non necessariamente alla domanda clinicamente rilevante.
L’introduzione del termine di interferenza non “penalizza” il TMD: rende esplicito il fatto che la stessa evidenza può essere condivisa da spiegazioni eziologiche concorrenti e che questa competizione riduce la sicurezza decisionale. In questo senso, la probabilità contestuale non misura più la coerenza interna di una classificazione, ma la sua affidabilità come guida clinica in presenza di alternative gravi.
Il valore del 9.56% non va quindi letto come una nuova stima di prevalenza, ma come un indicatore di instabilità diagnostica: un segnale quantitativo che avverte che il sistema decisionale sta operando in una regione di sovrapposizione ad alto rischio, dove la certezza numerica non equivale a sicurezza clinica.
E allora, che cosa stiamo davvero dicendo?
A questo punto il lettore potrebbe legittimamente chiedersi: abbiamo mostrato calcoli, probabilità, interferenze, matrici e crolli numerici impressionanti — ma qual è il punto clinico reale di tutto questo?
Il punto non è dimostrare che il formalismo classico “sbaglia”, né introdurre un linguaggio più sofisticato per il gusto della complessità. Il punto è più semplice e più scomodo:Il valore assoluto di un indice, anche quando statisticamente fondato, non è sufficiente a descrivere lo stato del sistema. L’ordine con cui l’informazione viene acquisita conta; il tempo che separa i test conta; la presenza di eziologie concorrenti conta. In questi scenari, la diagnosi non è una fotografia, ma un processo dipendente dal percorso.esistono contesti clinici in cui un’elevata certezza numerica non coincide con una diagnosi certa
Questo pone una serie di domande che non possono più essere eluse:
- ha senso affidarsi a un valore numerico scalare quando lo stato clinico evolve e si riorganizza nel tempo?
- cosa significa “certezza diagnostica” se l’esito dipende dall’ordine dei test?
- come distinguere una diagnosi corretta ma tardiva da una diagnosi realmente precoce?
- è possibile rappresentare lo stato clinico come qualcosa di più ricco di un numero: un vettore, una fase, una configurazione?
L’Indice nasce da queste domande, non come risposta definitiva, ma come tentativo operativo di dare forma quantitativa all’instabilità diagnostica. Non per sostituire i criteri esistenti, ma per segnalare quando il sistema clinico sta operando in una regione di sovrapposizione pericolosa, dove il valore assoluto smette di essere informativo e diventa necessario un concetto di stato.
Se il lettore è arrivato fin qui con una sensazione di disagio — la percezione che “qualcosa non torni” pur in presenza di numeri rassicuranti — allora il problema è stato posto correttamente. Le sezioni successive dell’Indice Ψ non faranno che esplorare sistematicamente questo disagio: i livelli di osservazione clinica, il limite del valore assoluto, la non-commutatività clinica, la natura vettoriale dello stato diagnostico e il Rumore ed il segnale criptato.
Questi capitoli non sono un abbellimento teorico, ma il percorso necessario per formalizzare la costruzione
dell’Indice
come strumento clinico: collaborativo, dinamico e deliberatamente non riducibile a una singola metrica scalare.
- ↑ NASEM Temporomandibular Disorders: Priorities for Research and Care The National Academies Press, Washington, DC (2020), 10.17226/25652
- ↑ B.J. Sessle. Chronic orofacial pain: models, mechanisms, and genetic and related environmental influences. Int J Mol Sci, 22 (2021), 7112, 10.3390/ijms22137112
- ↑ Sollecito T.P., Richardson R.M., Quinn P.D., Cohen G.S.: Intracranial schwannoma as atypical facial pain. Oral Surg Oral Med Oral Pathol. 1993;76:153-6.
- ↑ Shankland W.E.: Trigeminal neuralgia: typical or atypical? Cranio. 1993;11:108-12.
- ↑ Graff-Radford S.B., Solberg W.K.: Is atypical odontalgia a psychological problem? Oral Surg Oral Med Oral Pathol. 1993;75:579-82.
- ↑ Ruelle A., Datti R., Andrioli G.: Cerebellopontine angle osteoma causing trigeminal neuralgia: case report. Neurosurgery. 1994;35:1135-7.
- ↑ B.C. Cooper. Temporomandibular disorders: a position paper of the ICCMO. Cranio, 29 (2011), 237-244, 10.1179/crn.2011.034
- ↑ M.S. Nguyen et al. Occlusal support and temporomandibular disorders among elderly Vietnamese. Int J Prosthodont, 30 (2017), 465-470, 10.11607/ijp.5216
- ↑ M.S. Nguyen et al. The impact of occlusal support on temporomandibular disorders: a literature review. Proc Singap Healthc, 31 (2021), 1-12, 10.1177/2010105821102
- ↑ T.R. Walton, D.M. Layton. Mediotrusive occlusal contacts: best evidence consensus statement. J Prosthodont, 30(S1) (2021), 43-51, 10.1111/jopr.13328
- ↑ A. Kucukguven et al. Temporomandibular joint innervation: anatomical study and clinical implications. Ann Anat, 240 (2022), 151882, 10.1016/j.aanat.2021.151882
- ↑ E. Tervahauta et al. Asymmetries and midline shift in relation to TMD in a Finnish adult population. Acta Odontol Scand, 80 (2022), 1-11, 10.1080/00016357.2022.2036364
- ↑ R.B. Fillingim et al. Potential psychosocial risk factors for chronic TMD: OPPERA domains. J Pain, 12 (2011), T46-T60, 10.1016/j.jpain.2011.08.007
- ↑ G.D. Slade et al. Painful temporomandibular disorder: decade of discovery from OPPERA studies. J Dent Res, 95 (2016), 1084-1092, 10.1177/0022034516653743
- ↑ P. Svensson, F. Exposto. Commentary: overlaps among chronic pain conditions, but no news about causal relationships. J Oral Facial Pain Headache, 34(Suppl) (2020), s6-s8, 10.11607/ofph.2020.suppl.c2
- ↑ C.S. Stohler, G.A. Zarb. On the management of TMD: a low-tech, high-prudence approach. J Orofac Pain, 13 (1999), 255-261.
- ↑ J. Feng et al. Treatment modalities of masticatory muscle pain: network meta-analysis. Medicine (Baltimore), 98 (2019), e17934, 10.1097/MD.0000000000017934
- ↑ Z. Al-Ani. Occlusion and TMD: a long-standing controversy. Prim Dent J, 9 (2020), 43-48, 10.1177/2050168420911029
- ↑ C. Penlington et al. Psychological therapies for TMDs. Cochrane Database Syst Rev, Issue 8 (2022), CD013515, 10.1002/14651858.CD013515.pub2
- ↑ Martina K. Shephard & Gary Heir. Orofacial Pain in the Medically Complex Patient. Contemporary Oral Medicine, 26 January 2019.
- ↑ Kolmogorov A.N. Grundbegriffe der Wahrscheinlichkeitsrechnung. Springer-Verlag, Berlin (1933).