Spasmo emimasticatorio
Abstract
Questo capitolo ricostruisce il ragionamento diagnostico che conduce da una generica etichetta di “disfunzione masticatoria” a una diagnosi neuromotoria precisa: lo Spasmo Emimasticatorio (Hemimasticatory Spasm, HMS), presentato attraverso il percorso clinico di una paziente indicata come “Mary Poppins”. Sebbene la fenomenologia dell’HMS — contrazioni involontarie unilaterali dei muscoli masticatori — possa apparire clinicamente riconoscibile, la vera difficoltà non risiede nel nominare lo spasmo, bensì nell’eseguire una rigorosa diagnosi differenziale con condizioni che possono mimarlo o coesistere con esso, incluse lo spasmo emifacciale, lesioni centrali dell’angolo ponto-cerebellare, traumi dei nervi periferici, patologie demielinizzanti e neoplasie infiltrative o compressive.
Partendo dalla più ampia categoria dei disturbi del movimento indotti perifericamente, il capitolo sottolinea come i movimenti involontari anomali possano essere innescati da traumi ai nervi cranici o periferici o alle loro radici, ma possano anche essere generati o modulati da meccanismi centrali. Questo principio impone al clinico di mantenere un orizzonte diagnostico ampio. I tumori dell’angolo ponto-cerebellare — come schwannomi vestibolari, meningiomi o tumori epidermoidi — sono stati riportati come rare cause di spasmo emifacciale, attraverso meccanismi che includono il coinvolgimento vascolare, la compressione diretta del nervo o la distorsione del tronco encefalico. Il capitolo estende questo ragionamento al sistema trigeminale, evidenziando che gli schwannomi del trigemino, pur essendo rari, sono clinicamente rilevanti: possono presentarsi in modo atipico, persino come malocclusione indolore associata a debolezza masticatoria unilaterale, costringendo l’odontoiatria e la neurofisiologia a convergere nello stesso spazio diagnostico. Il neuroimaging rimane essenziale, ma deve essere interpretato all’interno di un quadro neurofunzionale e non come spiegazione autosufficiente.
Un secondo importante ambito della diagnosi differenziale riguarda le patologie demielinizzanti. La sclerosi multipla viene esaminata come archetipo di danno multifocale del sistema nervoso centrale, caratterizzato da espressione clinica variabile e da un’incertezza diagnostica non trascurabile. In particolare, la valutazione dei riflessi trigeminali — soprattutto il jaw jerk e il periodo silente masseterino — può rivelare il coinvolgimento del tronco encefalico in casi selezionati, talvolta quando altri riflessi risultano normali. Questo genera un dilemma clinicamente rilevante: quando vengono rilevate anomalie dei riflessi trigeminali, il clinico deve stabilire se esse riflettano una demielinizzazione centrale, una disfunzione delle branche motorie periferiche o un processo alternativo.
Il capitolo analizza poi i disturbi neoplastici e infiammatori in grado di produrre spasmi facciali o effetti perineurali, incluse le neoplasie delle ghiandole salivari come l’adenoma pleomorfo, per le quali la valutazione di imaging (TC vs RM) differisce nella definizione dei tessuti molli e nella valutazione di una possibile invasione perineurale. Infine, vengono introdotte la sclerodermia sistemica e localizzata, con particolare attenzione alla Morfèa come condizione documentata nella paziente, e vengono discussi i lavori che collegano la sclerodermia localizzata e l’emiatrofia facciale allo spasmo emimasticatorio. Sulla base di dati clinici ed elettrofisiologici trigeminali, la demielinizzazione focale delle branche motorie del trigemino e fenomeni eccitatori anomali vengono proposti come meccanismi plausibili.
Il “codice cifrato” diagnostico che organizza questa complessità viene identificato nella trasmissione efaptica: una comunicazione elettrica patologica tra elementi neurali adiacenti in assenza di un contatto sinaptico normale. Il capitolo si chiude collocando i meccanismi efaptici come ponte concettuale tra lo spasmo clinico, le asimmetrie riflesse e l’interpretazione neurofisiologica, preparando il lettore al capitolo dedicato alle due forme di trasmissione elettrica tra neuroni.
-
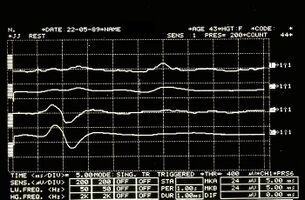
Figura 3: Riflesso mandibolare rilevato elettrofisiologicamente sul massetere destro (tracce superiori) e sinistro (tracce inferiori).
-
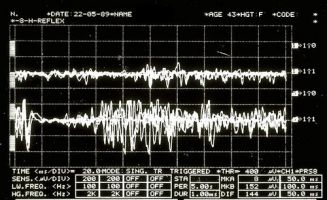
Figura 4: Periodo silente meccanico rilevato elettrofisiologicamente sul massetere destro (tracce sovrapposte superiori) e sinistro (tracce sovrapposte inferiori).
🧠 Three guiding questions (with essential answers)
1️⃣ Perché lo Spasmo Emimasticatorio è diagnostically impegnativo nonostante un aspetto clinico riconoscibile? — Perché lo spasmo masticatorio unilaterale può mimare o sovrapporsi allo spasmo emifacciale, a patologie demielinizzanti, a lesioni dei nervi periferici o a lesioni centrali, rendendo indispensabile una diagnosi differenziale accurata per evitare attribuzioni eziologiche errate e trattamenti inappropriati.
2️⃣ Perché i riflessi trigeminali sono cruciali nella diagnosi differenziale dei disturbi del movimento masticatorio? — Perché test elettrofisiologici come il jaw jerk e il periodo silente masseterino possono rivelare asimmetrie funzionali e anomalie di conduzione utili a distinguere tra demielinizzazione centrale, coinvolgimento delle branche motorie periferiche e fenomeni eccitatori anomali all’interno del sistema trigeminale.
3️⃣ Quale ruolo svolge la trasmissione efaptica nella fisiopatologia dello Spasmo Emimasticatorio? — La trasmissione efaptica fornisce una spiegazione meccanicistica dell’attività muscolare involontaria anomala, consentendo un accoppiamento elettrico patologico tra elementi neurali adiacenti e generando segnali eccitatori in assenza di una normale mediazione sinaptica.
If you already have an approved account, click on your profile icon and return to the Book Index to read the complete chapter.
To access the full content, you must sign in via LinkedIn and request approval.
Bibliography & references
- Jankovic J. Peripherally induced movement disorders. Neurol Clin. 2009 Aug;27(3):821–832. DOI: 10.1016/j.ncl.2009.04.005.
- Lee SH, Rhee BA, Choi SK, Koh JS, Lim YJ. Cerebellopontine angle tumors causing hemifacial spasm: types, incidence, and mechanism in nine reported cases and literature review. Acta Neurochir (Wien). 2010 Nov;152(11):1901–1908. DOI: 10.1007/s00701-010-0796-1.
- Peker S, Ozduman K, Kiliç T, Pamir MN. Relief of hemifacial spasm after radiosurgery for intracanalicular vestibular schwannoma. Minim Invasive Neurosurg. 2004 Aug;47(4):235–237. DOI: 10.1055/s-2004-818485.
- Bertot BE, Lo Presti M, Stormes K, Raskin JS, Jea A, Chelius D, Lam S. Trigeminal schwannoma presenting with malocclusion: A case report and review of the literature. Surg Neurol Int. 2020 Aug 8;11:230. DOI: 10.25259/SNI_482_2019.
- Agarwal A. Intracranial trigeminal schwannoma. Neuroradiol J. 2015 Feb;28(1):36–41. DOI: 10.15274/NRJ-2014-10117.
- Kamińska J, Koper OM, Piechal K, Kemona H. Multiple sclerosis – etiology and diagnostic potential. Postepy Hig Med Dosw. 2017 Jun 30;71:551–563. DOI: 10.5604/01.3001.0010.3836.
- Yates SK, Brown WF. The human jaw jerk: electrophysiologic methods to measure the latency, normal values, and changes in multiple sclerosis. Neurology. 1981 May;31(5):632–634. DOI: 10.1212/WNL.31.5.632.
- Koyuncu M, Seşen T, Akan H, Ismailoglu AA, Tanyeri Y, Tekat A, Unal R, Incesu L. Comparison of computed tomography and magnetic resonance imaging in the diagnosis of parotid tumors. Otolaryngol Head Neck Surg. 2003 Dec;129(6):726–732. DOI: 10.1016/j.otohns.2003.07.009.
- Machado RA, Moubayed SPM, Khorsandi A, Hernandez-Prera JC, Urken ML. Intermittent facial spasms as the presenting sign of a recurrent pleomorphic adenoma. World J Clin Oncol. 2017 Feb 10;8(1):86–90. DOI: 10.5306/wjco.v8.i1.86.
- Amaral TN, Peres FA, Lapa AT, Marques-Neto JF, Appenzeller S. Neurologic involvement in scleroderma: a systematic review. Semin Arthritis Rheum. 2013 Dec;43(3):335–347. DOI: 10.1016/j.semarthrit.2013.05.002.
- James W, Berger T, Elston D. Andrews’ Diseases of the Skin: Clinical Dermatology. 10th ed. Saunders; 2005. p.171. ISBN: 0-7216-2921-0.
- Kim HJ, Jeon BS, Lee KW. Hemimasticatory spasm associated with localized scleroderma and facial hemiatrophy. Arch Neurol. 2000 Apr;57(4):576–580. DOI: 10.1001/archneur.57.4.576.